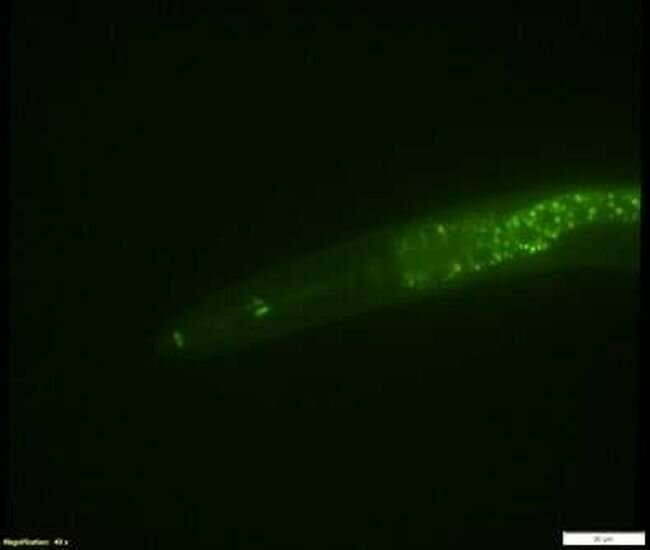
Una nueva técnica de edición de genes descubierta por investigadores de la UO reduce significativamente el tiempo dedicado a la investigación, lo que permite explorar varias áreas que antes no estaban disponibles. Gracias a este método, los biólogos ahora pueden comparar muchas versiones de un gen para encontrar mutaciones que den lugar a rasgos específicos y, al mismo tiempo, seguir su evolución a lo largo del tiempo.
Al realizar este tipo de investigación, los científicos han dado un paso importante hacia la identificación de mutaciones relevantes para la salud humana o la comprensión de los mecanismos subyacentes a las enfermedades humanas. Aunque ya se han desarrollado técnicas de edición masiva de genes para organismos unicelulares como bacterias y levaduras, esta es la primera vez que han sido posibles a esta escala en un animal.
La edición de genes da un paso adelante
“En biología pasamos mucho tiempo trabajando con mutantes genéticos. Pero en los animales estamos limitados por la cantidad de mutantes genéticos que podemos producir al mismo tiempo”, afirma el investigador. zach stevenson, quien ayudó a diseñar la técnica. "Esta es una nueva forma de superar ese cuello de botella".
Stevenson y sus colegas describen su nueva técnica en una preimpresión publicada en bioRxiv. Te lo enlazo aquí.
El sistema, desarrollado con el diminuto gusano C. elegans, también podría funcionar en otros animales de laboratorio, como moscas o ratones, dice Stevenson.
Porque es importante
Hay muchas razones por las que los científicos pueden querer tener la capacidad de crear muchas mutaciones genéticas al mismo tiempo. Por ejemplo, podrían estar editando una mutación que hace que un animal sea resistente a un fármaco específico, capaz de sobrevivir en determinadas condiciones o menos susceptible a una enfermedad.
Es posible que necesiten observar docenas o incluso cientos de posibles variaciones en un gen para encontrar la más efectiva.
La ingeniería de este tipo de edición. genética experimental es extremadamente lento en los animales. Cada cepa mutante, una colección de gusanos con una modificación genética predeterminada, debe crearse una por una. "Por lo general", dice Stevenson, "se necesitan entre siete y diez horas de práctica" para crear un único mutante. Este sistema recién descubierto le permite “crear decenas de miles” en el tiempo que ahora lleva crear sólo tres o cuatro.
Cómo funciona el nuevo método
Para acelerar las cosas, Stevenson y sus colegas diseñaron una forma de comprimir cientos o incluso miles de posibles mutaciones en una única "biblioteca". Cada libro de la biblioteca es un pequeño fragmento de código genético, en sí mismo insignificante y no funcional. Cada fragmento encaja en un “nicho” diseñado en el gen al que se dirige.
Este diseño permite un verdadero cambio de paradigma: en lugar de inyectar individualmente a muchos gusanos diferentes versiones de un gen, los investigadores pueden inyectar toda la biblioteca de mutaciones en un solo gusano.
Luego, cuando el gusano se reproduce, la biblioteca se expande. En cada descendiente, se selecciona aleatoriamente un libro de la biblioteca de mutaciones para complementar el gen objetivo. El resultado: una colección de gusanos que tienen diferentes mutaciones genéticas seleccionadas al azar.
Los investigadores llamaron a su técnica TARDIS, un guiño lúdico a la cabina de policía que viaja en el espacio y el tiempo del Dr. Who. Aquí significa Matrices transgénicas que dan como resultado diversidad de secuencias integradas.
Posibles aplicaciones de la edición 2.0
Los investigadores probaron TARDIS con un gen que les da a los gusanos resistencia a los antibióticos. Pero ven amplias aplicaciones para la biología en general, incluida la investigación en otros organismos modelo.
Podría ser particularmente útil para estudiar interacciones entre proteínas o señalización entre células, sugiere el profesor investigador de la UO Esteban Banse, que ayudó a desarrollar la TARDIS. Tales interacciones son a menudo relevantes para comprender las enfermedades, pero los científicos pierden un contexto importante al estudiarlas en levaduras o bacterias, dijo Banse.
"Ahora podemos hacer estas cosas en un modelo animal". Y luego en el hombre.